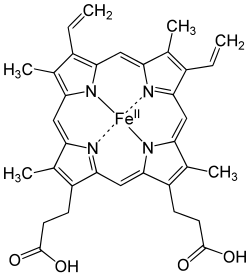
Гемы (от др.-греч. ἁίμα — «кровь») — комплексные соединенияпорфиринов с двухвалентным железом, несущие один или два аксиальных лиганда[1]. Гемы выступают в роли простетических групп (небелковых частей) белков — гемопротеинов (гемоглобинов, миоглобина, цитохромов и др.). Гемы являются одной из разновидностей коферментов (Кофакторы ферментов).
Общее описание
Гем — общее название для ряда сходных веществ. Наиболее распространённым гемом является гем B — железо-хелатированный комплекс протопорфирина IX, входящий в состав гемоглобинов, миоглобинов и цитохромов.
Известен ряд различных гемов, отличающихся заместителями порфиринового ядра:
Позвоночные синтезируют гем из более простых азотистых соединений (глицина и сукцината) и из резервного железобелкового комплекса — ферритина, находящегося в селезёнке, печени, костном мозге. Гем, выделенный из крови различных позвоночных животных, имеет одинаковую химическую структуру.
Свободный гем легко окисляется на воздухе до гематина, в котором атом железа трёхвалентен. Многолетние исследования структуры гема завершились синтезом гемина — солянокислого гематина (Х. Фишер, 1929).
Гем является промежуточным продуктом метаболизма гемоглобина в вызывающих маляриюплазмодиях (род Plasmodium), где он превращается в гематин. Для плазмодиев гем токсичен[2].
См. также
Примечания
- ↑Hemes (heme derivatives) // IUPAC Gold Book. Дата обращения: 19 марта 2012. Архивировано 20 октября 2012 года.
- ↑Лосева П. Колесо злоключений // N + 1. — 2020. — 9 июня.
