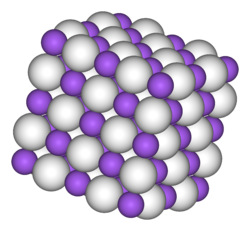
Гидри́д на́трия — сложноенеорганическое вещество с химической формулойNaH. Представляет собой белый порошок, реагирует с водой; ядовит.
Описание
При стандартных условиях гидрид натрия представляет собой бесцветные кубические кристаллы с кристаллической решёткой типа . Является сильным восстановителем. Воспламеняется в атмосфере некоторых галогенов (фтор, хлор), а также при 230 °C в кислороде. При нагревании до 300 °C в вакууме гидрид натрия разлагается. Реагирует с водой, спиртами, жидким аммиаком, ацетиленом, трифторидом бора, оксидом углерода (IV).
Получение
- Нагревание натрия до 360—400 °C при пропускании водорода:
- Взаимодействие натрия с гидроксидом натрия[1]:
- Разложение амида натрия.
Химические свойства
- Бурное взаимодействие с водой с образованием щёлочи — гидроксида натрия:
- Разложение при сильном нагревании в вакууме:
- Окисляется кислородом до гидроксида натрия:
- С неметаллами образует соответствующие натриевые соли:
- Реагирует с углекислым газом с образованием формиата:
Сферы применения
Гидрид натрия применяют для очистки железа от магнетита. В органической химии он используется в качестве конденсирующего и полимеризующего агента. Раствор в гидроксиде натрия применяют для снятия окалины с тугоплавких металлов и специальных сталей.
Биологическое действие
Вещество токсично. При контакте гидрида натрия с водой образуется натриевая щёлочь (едкий натр).
ПДК в воде — 200 мг/дм³ (по ионам натрия), 2-й класс опасности в соответствии с гигиеническими нормативами.
При контакте со слизистыми оболочками гидрид натрия может вызвать щелочной ожог; коррозионно-активен.
Примечания
- ↑Pradyot Patnaik. Handbook of Inorganic Chemicals. — McGraw-Hill, 2003. — С. 850. — 1086 с. — ISBN 0-07-049439-8.
- ↑Лидин, 2000, с. 19.
Литература
- Химические свойства неорганических веществ / под ред. Р.А. Лидина. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.